肿瘤标志物学术大会 CCTB大会 2022
CCTB 2022:https://biomarker2022.sciconf.cn
参加肿瘤标志物的大会,好几个会议同步进行,来演讲的人都是业界的专家,水平很高,虽然大部分报告都是科研形式的汇报,和产业汇报不一样,但同样给人启发。


CCTB 2022:https://biomarker2022.sciconf.cn
参加肿瘤标志物的大会,好几个会议同步进行,来演讲的人都是业界的专家,水平很高,虽然大部分报告都是科研形式的汇报,和产业汇报不一样,但同样给人启发。

保存几张1D卷积的图和文章,方便以后查找,摘自互联网。说不准以后搞深度学呢🫠🙃卷的结果就是以后不上人工智能都不要意思说自己是搞生信的。
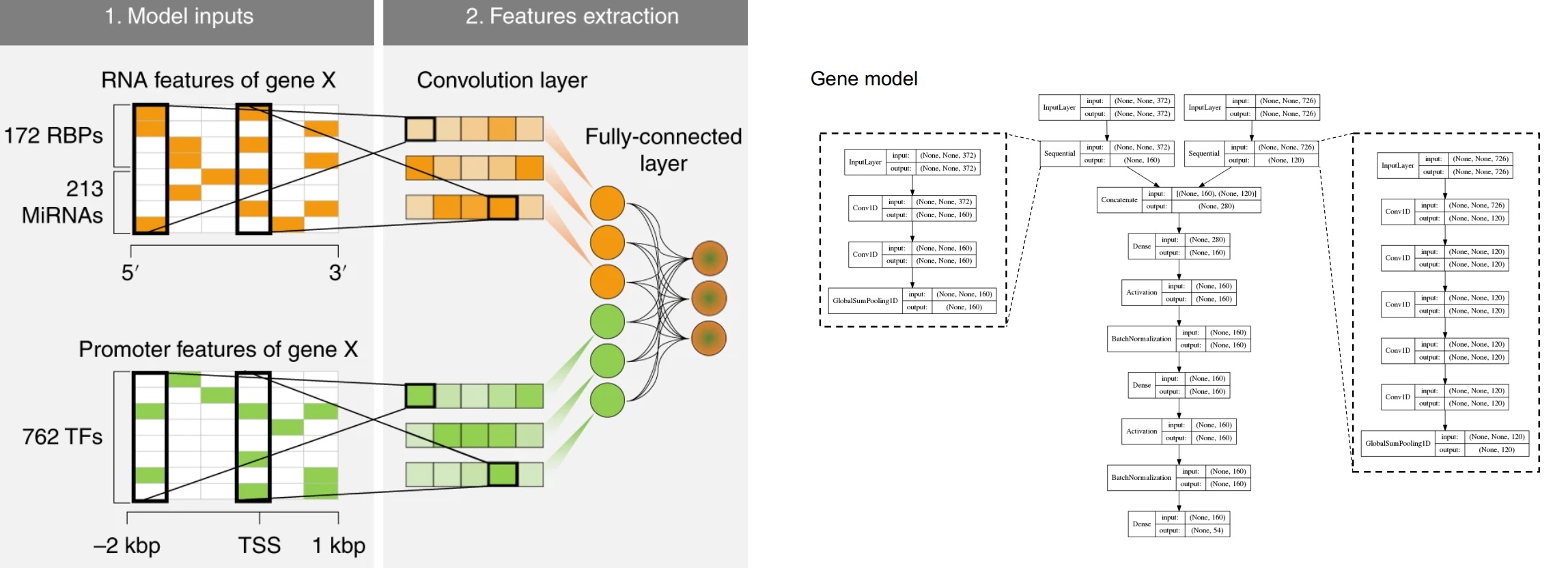
主要是看到一篇文章,用了卷积神经网络,我一直就好奇组学数据怎么做卷积,所以就看了下文章,发现用的是Conv1D。(不知道理解的对不对)对于1D卷积Conv1D而言,如果卷积核kernel size是2的话,最终会生成一个 “行数-kernel size+1“的向量,如果数据分批给的话,就有batch,比如如果样本是21000,batch size是128的话,每个batch有165个样本,所以Nature Machine Intelligence的附图 Fig. 10这篇文章还进行了BatchNormalization。
Samples = 21000,batch_size=128-> training_sample for each epoch =21000/128 = 164.06 ~= 165
filters可以指定多次卷积(相同kernel size),这样可以生成二维的数据。
| Args | https://www.tensorflow.org/api_docs/python/tf/keras/layers/Conv1D |
|---|---|
filters |
Integer, the dimensionality of the output space (i.e. the number of output filters in the convolution). |
kernel_size |
An integer or tuple/list of a single integer, specifying the length of the 1D convolution window. |
Deep learning decodes the principles of differential gene expression
分析的代码已经调试好,但分析的时间较长;
后端启动jupyter notebook后,奈何网络不稳定,notebook经常掉线,跑到一半的程序就断掉了;
服务器其他人的jupyter notebook的端口如果和我的一样,别人启动jupyter notebook后,我正在用的端口就会往后变。
于是我就想,能否在终端直接运行.ipynb文件,这样我就可以加nohup命令了,或者把ipynb的代码转成python,我nohup运行python也行。
基于以上情况,我google到了nbconvert。
nbconvert的github地址:https://github.com/jupyter/nbconvert
jupyter nbconvert通过模版引擎jinja将ipynb文件转成其他格式的文件,包括
此外nbconvert还有另外一个功能就是通过–execute选项在终端执行ipynb文件
|
|
|
|
上面是格式转换,在转换的过程中,比如转pdf、latex的时候,可能还需要额外的包,比如pandoc等,还需要额外安装。可以参考https://nbconvert.readthedocs.io/en/latest/index.html
jupyter nbconvert还有个功能就是执行ipynb格式的文件,如下
|
|
假设我想把通过运行jupyter nbconvert执行ipynb文件的过程更简单点,可以通过在.profile里面设置命令的别名
|
|
当进行Isoseq的样本测了多次,或者多个run时,可能会碰到合并subreads.bam文件。我倾向先合并再往后分析,兼容以前的流程,避免分别分析再合并会遇到其他错误。Pacbio Isoseq的下机数据格式已经从h5变成了subreads.bam,合并其实很简单,和samtools类似,但得用pacbio的工具才行,当然还要建立index生成pbi文件,也是用pacbio的工具。
|
|
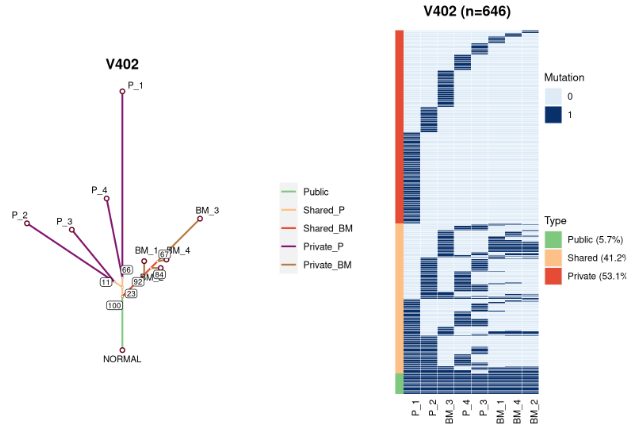
Variant allele fraction or frequency (VAF): the fraction of mutated reads for a given variant, which is a readout for the proportion of DNA mutated in the sequenced tissue.
测序时特定位点突变的reads数比上总的reads数,可以从VCF中获得。
Cancer cell fraction (CCF): the fraction of cancer cells from the sequenced sample carrying a set of SNVs.
携带突变的癌细胞比例,可以通过pyclone(https://github.com/Roth-Lab/pyclone-vi)或sciclone(https://github.com/genome/sciclone)计算。
$$ CCF = VAF *\frac{1}{p}[pCN_t + CN_n(1-p)] $$
VAF: corresponds to the variant allele frequency at the mutated base
p: the tumor purity肿瘤纯度
CNt: the tumor locus specific copy number所在位置的拷贝数
CNn: the normal locus specific copy number (CNn was assumed to be 2 for autosomal chromosomes)正常样本的拷贝数